Abstrakcyjny
Selektywny transport jonów leży u podstaw podstawowych procesów biologicznych zapewniających efektywną konwersję energii i propagację sygnału. Naśladowanie tych „jonów” w syntetycznych kanałach nanofluidycznych staje się coraz bardziej obiecujące w realizacji samowystarczalnych systemów poprzez pozyskiwanie czystej energii z różnorodnych środowisk, takich jak światło, wilgoć, gradient zasolenia itp. W tym miejscu przedstawiamy przestrzennie nanoograniczoną strategię separacji jonów, która umożliwia pozyskiwanie energii elektrycznej z adsorpcji CO2 . Ten przełom polega na opracowaniu generatorów na bazie kompozytu nanoarkuszowo-hydrożelowego (NAH), w których przeciwnie naładowane jony są uwalniane w wypełnionych wodą kanałach hydrożelowych po adsorbowaniu CO2 . Dostrajając wielkość jonów i interakcje między kanałami jonowymi, uwolnione kationy w skali stu nanometrów są przestrzennie ograniczone w sieci hydrożelowej, podczas gdy aniony w skali ångströma przechodzą bez przeszkód. Prowadzi to do niemal idealnego rozdzielenia anionów/kationów w generatorze z selektywnością (D - /D + ) do 1,8 × 10 6 , umożliwiając konwersję na zewnętrzną energię elektryczną. Przy wzmocnieniu poprzez połączenie wielu zaprojektowanych generatorów, indukowany separacją jonów prąd o napięciu sięgającym 5 V jest wykorzystywany do zasilania urządzeń elektronicznych. W badaniu tym przedstawiono skuteczną strategię przestrzennego nanoograniczenia na potrzeby szeroko wymaganej, wysoce precyzyjnej separacji jonów, zachęcając do stosowania techniki ujemnej pod względem emisji dwutlenku węgla z jednoczesną adsorpcją CO 2 i wytwarzaniem energii.
Wstęp
Globalne ocieplenie spowodowane emisją gazów cieplarnianych 1 , 2 , 3 , 4 , przede wszystkim emisją dwutlenku węgla (CO 2 ) w wyniku działalności człowieka 4 , 5 , 6 , jest jednym z kluczowych wyzwań naszych czasów. Oczekuje się, że strategie wychwytywania, utylizacji i składowania dwutlenku węgla (CCUS) odegrają kluczową rolę w łagodzeniu tego wyzwania. Obecne technologie CCUS są jednak nadal energochłonne i kosztowne, co zagraża ich zrównoważeniu środowiskowemu i gospodarczemu 7 , 8 , 9 . Obecnie najbardziej dostępną na rynku opcją jest chemiczna adsorpcja CO 2 , podczas której CO 2 jest adsorbowany przez adsorbenty wodne, takie jak alkanoloaminy lub aminy 10 . Ujemna zmiana entalpii (Δ H ) procesu adsorpcji chemicznej, na co wskazuje jego spontaniczny i egzotermiczny charakter, może służyć jako cel pozyskiwania energii w celu zwiększenia jego efektywności energetycznej 5 , 8 .
Przy wyborze wykonalnego podejścia do pozyskiwania energii z CO 2 można kierować się procesami „jonowymi” opartymi na przyrodzie 11 . Biologiczne procesy konwersji energii lub propagacji sygnału opierają się zasadniczo na regulowanym transporcie jonów w biokanałach 11 , 12 , 13 . Zachęciło to pojawiające się postępy w selektywnym transporcie jonów w syntetycznych kanałach nanofluidycznych w celu pozyskiwania energii elektrycznej ze źródeł niekonwencjonalnych 14 . Urządzenia tej techniki polegają na tworzeniu kierunkowej separacji jonów w sztucznych kanałach w odpowiedzi na zewnętrzne gradienty środowiska, na przykład ciepło 15 , ciśnienie 16 , 17 , zasolenie 18 , 19 , wilgoć 20 , 21 , 22 , światło 23 itp. Środowisko zewnętrzne napędza naładowane jony dyfundują przez kanały jonowe obecne w generatorach. Kanały jonowe są wstępnie zaprojektowane do transportu przeciwnie naładowanych jonów z rozróżnialnymi prędkościami, co prowadzi do wytworzenia wypadkowego prądu dyfuzyjnego i różnicy potencjałów elektrycznych w generatorze 21 , 24 .
W dostępnej na rynku chemicznej adsorpcji CO 2 roztwory amin mogą generować przeciwnie naładowane jony po absorpcji CO 2 w następujący sposób: CO 2 + R-NH 2 + H 2 O ⇌ R-NH 3 + + HCO 3 - (Równanie 1), jeśli jony te są skutecznie oddzielane, nadają się również do wytwarzania energii elektrycznej, jak wykazano niedawno 8 , 25 , 26 . Jednakże dodatnio naładowane jony amin i ujemnie naładowane jony wodorowęglanowe powstające w konwencjonalnym procesie adsorpcji CO2 mają podobne rozmiary na poziomie molekularnym i są dobrze wymieszane, co sprawia, że ich skuteczna separacja stanowi wyzwanie 10 , 27 , 28 . Zależność wyłącznie od dodatnio naładowanej membrany rozdzielającej dała selektywność mobilności wynoszącą 2,5 pomiędzy jonami HCO 3 - i R-NH 3 + 26 , czyli znacznie niższą wielkość w porównaniu z tym, co osiągnięto w procesie wytwarzania energii osmotycznej 19 . Sprostanie temu wyzwaniu mogłoby potencjalnie ułatwić dążenie do wydajnej konwersji energii i wystarczającej gęstości mocy w tej obiecującej dziedzinie.
Tutaj przedstawiamy generator na bazie kompozytu NAH, który może realizować precyzyjną separację jonów w swoich wewnętrznych kanałach w celu generowania energii elektrycznej bezpośrednio z adsorbowania CO 2 (rys. 1a ). Aby przezwyciężyć podobieństwo wielkości jonów generowanych przez tradycyjne adsorbenty, adsorbenty nanokompozytowe syntetyzuje się poprzez szczepienie cząsteczek polietylenoiminy (PEI) z licznymi grupami -NH/-NH2 w celu adsorpcji CO2 na dwuwymiarowym (2D) heksagonalnym azotku boru (h- BN) nanocząstki, tworzące nanocząstki h-BN funkcjonalizowane PEI (h-BN-NH2 ) (ryc. 1b i , ryc. uzupełniająca 1 ). Po adsorbcji CO 2 nanokompozyty h-BN-NH 2 uwalniają w hydrożelu dodatnio naładowane jony NH 3 + związane z h-BN o rozmiarach w skali stu nanometrów (100–300 nm) i ujemne wolne jony HCO 3 - w skali Å kanały, tworząc między nimi różnicę wielkości przekraczającą dwie wielkości (ryc. 1b ii ). Ponieważ wydłużony szkielet h-BN składający się z jonów dodatnich jest uwięziony przez matrycę hydrożelową agarozową, podczas gdy ujemne jony HCO 3 - pozostają swobodnie w połączonych ze sobą kanałach wypełnionych wodą, te przeciwnie naładowane jony dyfundują przez generator z niezwykłą różnicą szybkości ( >10 6 ). (Rys. 1b iii ). Taka różnica szybkości dyfuzji jest przekształcana na energię elektryczną i dalej wzmacniana w celu zasilania zewnętrznych urządzeń elektronicznych. W badaniu tym wykorzystano gazowy CO 2 jako cel pozyskiwania energii. Zademonstrowane strategie inżynierii jonowej mogą przyczynić się do rozwoju innych zastosowań związanych z separacją jonów w zakresie energii, zasobów i ochrony środowiska.
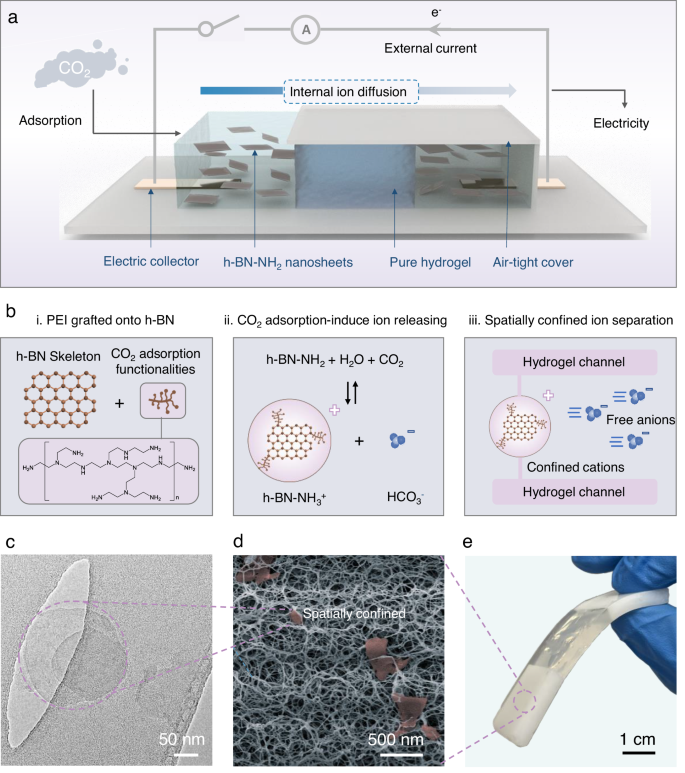
a Schematyczna ilustracja prototypowego generatora prądu NAH. Generator został celowo zaprojektowany z symetryczną strukturą pomiędzy dwoma kolektorami elektrycznymi, aby zapewnić zrównoważony potencjał chemiczny w generatorze na początkowym etapie. b Proces separacji jonów indukowany jest wytwarzaniem energii elektrycznej z adsorpcji CO 2. Rozpoczyna się od (i) szczepienia PEI na nanocząsteczkach azotku boru w celu uzyskania adsorbentów h-BN-NH 2 , (ii) adsorpcja CO 2 indukuje uwalnianie kationów przez jony ( h-BN-NH 3 + ) i aniony (HCO 3 - ), (iii) kationy w stu nanometrach są przestrzennie ograniczone, podczas gdy aniony mogą swobodnie przemieszczać się w obrębie kanałów hydrożelu, co prowadzi do precyzyjnego rozdziału jonów. c Obraz TEM złuszczonych i funkcjonalizowanych nanocząstek h-BN- NH2 . d Obraz SEM struktury przekroju poprzecznego kompozytu NAH. Czerwone krążki to nanocząsteczki h-BN-NH2 uwięzione w sieci hydrożelowej. e Zdjęcie generatora prądu NAH.
Wyniki i dyskusja
Racjonalne projektowanie i wytwarzanie generatora energii elektrycznej
Nanocząstki h-BN-NH 2 , będące kluczowym składnikiem generatora prądu NAH, otrzymano metodą lepkiej eksfoliacji, jak podano w naszej poprzedniej pracy 29 . Proces obejmował mielenie kulowe warstwowego h-BN i płynnego PEI o ultrawysokiej lepkości w celu jednoczesnego złuszczania i funkcjonalizacji. Wysoka lepkość PEI skutecznie rozbija i rozwarstwia warstwowe, masowe cząstki h-BN, a tymczasem cząsteczki PEI z gotowymi do reaktywności grupami aminowymi są szczepione na świeżo złuszczonych nanocząsteczkach h-BN w drodze reakcji mechanochemicznych 30 . Powstały produkt nazwano h-BN-NH2 , który zebrano i przepłukano wodą w celu usunięcia wolnych cząsteczek PEI. Grube płatki h-BN, które nie zostały dostatecznie złuszczone, usunięto w procesie wirowania. Obrazy z transmisyjnego mikroskopu elektronowego (TEM) pokazują, że powstałe nanocząstki h-BN mają wielkość boczną w zakresie od ~100 do 300 nm (ryc. 1c , ryc. uzupełniające 2 , 3 ). Analiza termograwimetryczna i elementarna ujawnia również, że cząsteczki PEI związane z nanocząsteczkami h-BN stanowią 7,92% wag. produktu końcowego (tabela uzupełniająca 1 , ryc. uzupełniająca 4 ). Struktura krystaliczna sieci BN została zachowana nawet po złuszczaniu i szczepieniu PEI poprzez wiązanie chemiczne (rysunek uzupełniający 5 ), jak pokazano przez charakterystyczne piki dyfrakcji promieni rentgenowskich przy 26,2 ° i 42,8 °, odpowiadające (002) i (100) płaszczyzny sześciokątnego azotku boru (rysunek uzupełniający 6 ). Co więcej, piki dyfrakcji promieni rentgenowskich (XRD) złuszczonego h-BN wykazują znacznie zmniejszoną intensywność i poszerzoną szerokość, co wskazuje na pomyślne złuszczanie pod względem wielkości bocznej i liczby warstw h-BN.
Aby stworzyć sztuczne kanały jonowe dla generatora prądu, jako matrycę wybrano hydrożel agarozowy, zawierający ~98% wag. wody, ze względu na jego wysoce porowatą strukturę z odpowiednią wielkością porów, która jest wystarczająco duża, aby transportować jony wodorowęglanowe, ale zbyt mała dla h- BN-NH 3 + nanocząsteczki umożliwiające swobodne przenikanie. Roztwór mieszaniny nanocząstek h-BN-NH2 i agarozy wlano kroplowo do formy z polidimetylosiloksanu (PDMS) i poddano termoreaktywnej przemianie zol-żel w celu wytworzenia elastycznej folii hydrożelowej (ryc. 1d, e ). Jonowe cząsteczki PEI szczepione na nanocząsteczkach h-BN poprawiają dyspergowalność nanocząsteczek w roztworze agarozy w porównaniu z czystym hydrofobowym h-BN 30 (ryc. 1d, e , ryc. uzupełniająca 7 ). Cząsteczki agarozy tworzą trójwymiarową, wzajemnie połączoną macierz siatkową o średniej średnicy 102 nm, wynikającą z wydłużonych hydrofilowych łańcuchów polimeru (ryc. 1d , ryc. uzupełniająca 3 ). Sieciowanie między/wewnątrzłańcuchowe uzyskano poprzez wplatanie grup funkcyjnych (-OH) cząsteczek agarozy w skoordynowaną sieć wiązań wodorowych 31 . Unikalne właściwości matrycy hydrożelowej zapewniają dużą wytrzymałość mechaniczną i dużą elastyczność kształtu. Jak pokazano na ryc. 1a , w celu skonstruowania prototypowego generatora energii elektrycznej NAH, dwa hydrożele NAH, służące odpowiednio jako zbiorniki uwalniające i odbierające jony, łączy się z czystym hydrożelem agarozowym, który działa jako szybkie kanały jonoselektywne.
Wytwarzanie energii elektrycznej z adsorpcji CO 2
Aby ocenić zdolność wytwarzania energii elektrycznej generatora prądu NAH, umieszczono go w skrzyni testowej (50 na 25 cm, rys. uzupełniająca 8 ) z wlotem CO2 . Strona zbiornika odbierająca jony została przykryta, natomiast strona zbiornika uwalniająca jony została wystawiona na działanie gazowego CO2 . Aby rozpocząć badanie, do komory testowej wprowadzano CO2 w ilości 2,5 l/min przez 3 minuty. Po zasilaniu CO 2 napięcie jałowe ( V OC ) generatora energii elektrycznej NAH osiągnęło wartość szczytową około 80 ± 10 mV w ciągu 1 do 2 godzin (rys. 2a ), a następnie stopniowo spadło do niewykrywalnego poziomu w ciągu około 15 godzin, potwierdzające, że energia elektryczna została wytworzona w wyniku adsorpcji CO2 . Następnie do skrzynki ponownie wprowadzono gazowy CO2, aby rozpocząć kolejny cykl testowy. Stwierdzono , że wytwarzanie energii elektrycznej jest solidne, a szczytowa wartość VOC utrzymuje się na poziomie 80 ± 10 mV w pięciu kolejnych testach trwających 60 godzin. Prąd zwarciowy ( ISC ) zachowywał się podobnie do VOC , osiągając wartość szczytową około 150 ± 20 nA przez 1 do 2 godzin , po czym powoli spadał do 0 w ciągu kolejnych 5 do 10 godzin (ryc. 2b ). Jednakże, w przeciwieństwie do VOC , pik ISC zanikał po każdym cyklu adsorpcji CO2 , a pik ISC w 5. cyklu był tylko o połowę mniejszy niż w 1. cyklu . Do badania VOC prąd całkowity ustawiono na 0, co równa się nieskończonej rezystancji obciążenia zewnętrznego (R do ∞), podczas gdy na całkowitą rezystancję badania I SC wpływa jedynie rezystancja wewnętrzna generatora. Tym samym niższa rezystancja całkowita podczas testów ISC doprowadziła do wyższego prądu rozładowania , a tym samym widocznego spadku wydajności w porównaniu z testami VOC 20 , 24 .
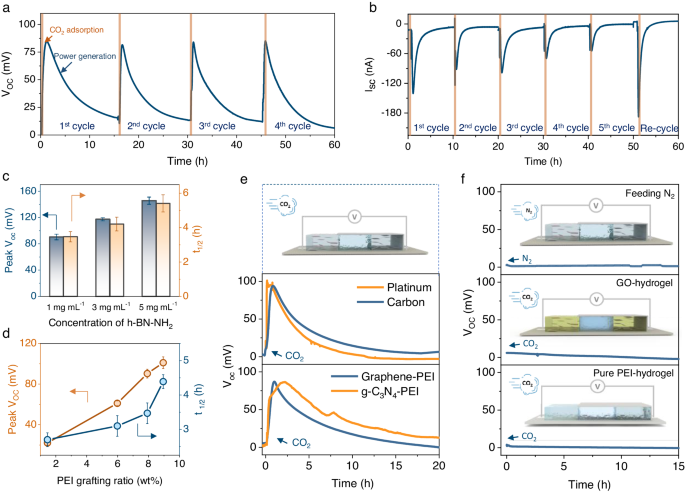
a Napięcie obwodu otwartego generatora prądu NAH wywołane cykliczną adsorpcją CO2 . b Cykliczny prąd zwarciowy generatora prądu NAH wywołany adsorpcją CO2 . Zastosowano zmianę pH w celu odzyskania wytwarzanej energii po piątym cyklu . CO2 wprowadzano do komory testowej z szybkością 2,5 l min -1 przez 3 minuty w każdym cyklu, zarówno w przypadku testów VOC , jak i I SC . c Wytwarzanie energii elektrycznej w kategoriach szczytowego VOC i czasu połowicznej wartości (t 1/2 ) indukowanego potencjału obwodu otwartego w funkcji stężenia nanocząstek h-BN-NH 2 w hydrożelu agarozowym. d Wytwarzanie energii elektrycznej w kategoriach szczytowego VOC i czasu połowicznej wartości (t 1/2 ) indukowanego potencjału obwodu otwartego jako funkcja stosunku wagowego funkcyjności PEI na nanoarkuszach h-BN . Słupki błędów to odchylenia standardowe z trzech testów. e Wytwarzanie energii elektrycznej przy użyciu elektrod węglowych i platynowych do zbierania sygnałów elektrycznych (panel środkowy) oraz Wytwarzanie energii elektrycznej przy użyciu grafenu funkcjonalizowanego PEI (Graphene-PEI) i graficznego azotku węgla funkcjonalizowanego PEI (gC 3 N 4 -PEI) (panel dolny). f Wytwarzanie energii elektrycznej w różnych eksperymentach kontrolnych: użycie N 2 do zastąpienia CO 2 jako gazu zasilającego do testów (górny panel), zastąpienie nanocząstek h-BN w generatorze nanocząsteczkami tlenku grafenu (środkowy panel) i czystymi cząsteczkami PEI (dolny panel) płyta).
Zaobserwowany zanik I SC wymaga zastosowania odpowiedniej metody regeneracji, aby zapewnić możliwość ponownego użycia generatora prądu NAH. Odnosząc się do wykresu Bjerruma, zaadsorbowany CO 2 występuje głównie w postaci jonów HCO 3 - w zakresie pH od 6,0 do 9,0. Biorąc pod uwagę środowisko wodne generatora energii elektrycznej NAH, powszechnie przyjęta strategia zmiany pH powinna umożliwiać usuwanie CO2 i regenerację generatora energii elektrycznej NAH 5 , 8 . Podczas procesu desorpcji przy zmiennym pH jony HCO 3 - mogą przejść do jonów CO 3 2 - jeśli wartość pH wzrośnie powyżej 10,0, umożliwiając sekwestrację poprzez reakcję z Ca 2+ z utworzeniem wytrąceń CaCO 3 25 . Alternatywnie, obniżenie wartości pH poniżej 4,0 powoduje przekształcenie jonów HCO 3 - w gazowy CO 2 , który można zebrać i wykorzystać 32 . Regenerację przeprowadzono poprzez zanurzenie generatora w alkalicznym roztworze buforowym (pH=10). Wyniki pokazują, że sygnały ISC i VOC można w pełni przywrócić do ich początkowych poziomów poprzez zmianę pH po pięciu cyklach adsorpcji i rozładowania (patrz ostatni cykl regeneracji na ryc. 2b i ryc . uzupełniającym 9 ).
Wytwarzanie energii elektrycznej przez generator NAH można łatwo zwiększyć poprzez zwiększenie gęstości miejsc adsorpcji CO 2 w generatorze NAH poprzez zwiększenie stężenia nanocząstek lub zwiększenie współczynnika szczepienia PEI h-BN- NH2 . Zwiększenie stężenia nanocząstek h-BN-NH 2 w hydrożelu NAH z 1 mg mL −1 do 5 mg mL −1 skutkowało wzrostem V OC z 90,4 mV do 145,7 mV z wydłużonym okresem połowicznej wartości V oc od 3,5 godziny do 5,4 godziny (ryc. 2c ). Nie uzyskano dalszej znaczącej poprawy poprzez zwiększenie stężenia do 10 mg ml -1 (rysunek uzupełniający 10 ). Podniesienie współczynników szczepienia PEI nanocząstek h-BN-NH2 z 1,46% wag. do 8,95% wag. zwiększyło VOC pięciokrotnie , a okres połowicznej wartości również wydłużył się ponad dwukrotnie (ryc. 2d ).
Aby lepiej zrozumieć pochodzenie wytwarzania energii elektrycznej, generator energii elektrycznej NAH został przetestowany w różnych warunkach. Po pierwsze, srebrne elektrody generatora prądu zastąpiono odpowiednio elektrodami z węgla obojętnego i platynowanego tytanu. Urządzenia wykorzystujące elektrody obojętne nadal wytwarzały prąd o szczytowej wartości Voc wynoszącej ~90 mV (ryc. 2e ). Wykluczają one możliwość, że energia elektryczna pochodzi z reakcji chemicznych zachodzących na elektrodach. Po drugie, kiedy zastąpiliśmy CO2 N2 jako gazem zasilającym, nie wykryto żadnych wyraźnych sygnałów elektrycznych (rys. 2f ), co wskazuje , że energia elektryczna została wygenerowana w wyniku adsorpcji CO2 .
Aby zbadać znaczenie szkieletów 2D nanocząstek h-BN-NH2 w matrycy hydrożelowej, dostosowaliśmy składniki hydrożelu NAH. Gdy grafen funkcjonalizowany PEI i grafitowy azotek węgla (gC 3 N 4 ), które mają strukturę podobną do nanocząstek h-BN-NH 2 , zastosowano jako nanonapełniacze w hydrożelu, tak skonstruowane generatory miały podobną wydajność do h-BN- Generator NH2 (ryc. 2e ). Jednakże, gdy zastosowano nanocząstki tlenku grafenu (GO) z grupami -OH/-COOH, w identycznych warunkach pracy nie wygenerowano prądu, co podkreśla krytyczną rolę grup -NH/-NH2 ( rys. 2f ). Ponadto, gdy do zastąpienia nanocząstek 2D h-BN-NH2 użyto czystego ciekłego PEI , generator również nie wygenerował energii elektrycznej (ryc. 2f ). Wyniki te pokazują, że duży rozmiar fizyczny nanocząstek (setki nanometrów) i liczne grupy aminowe są niezbędne do wytwarzania energii elektrycznej w generatorze NAH.
Zdolność adsorpcji CO2 nanocząstek h-BN-NH2 zmierzono jak pokazano na Fig. 3a . Wyniki pokazują, że nanocząstki h-BN-NH2 szczepione 7,92% wag. grup funkcyjnych PEI wykazują zdolność adsorpcji CO2 wynoszącą 0,238 mmol g -1 w standardowej temperaturze i ciśnieniu, podczas gdy h-BN w masie nie wykazuje mierzalnej zdolności adsorpcji CO2 . Aby potwierdzić wytwarzanie równomolowych jonów aminowych i wodorowęglanowych, monitorowano zmianę pH wodnego roztworu h-BN-NH2 podczas procesu adsorpcji CO2, wykazując szybki spadek z 8 do 4,5 w ciągu kilku minut ( Rys . 3b ) . Uwalnianie jonów w wyniku adsorpcji jest dodatkowo potwierdzone trzykrotnie wyższą przewodnością jonów obserwowaną w roztworze nanoarkuszów barbotowanym CO2 w porównaniu z N2 . (Rys. 3c i uwaga dodatkowa 3 ).
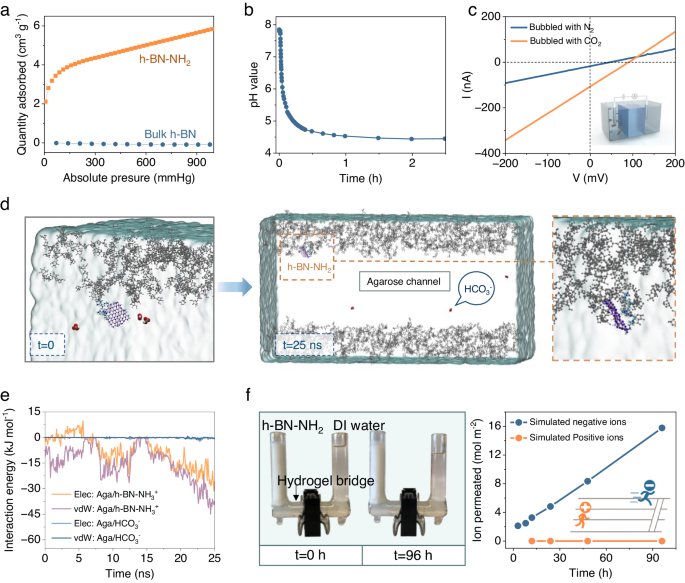
a Porównanie izoterm adsorpcji (293,15 K) CO2 przez nanocząstki h-BN-NH2 i h-BN w masie, zmierzone metodą analizy Brunauera-Emmetta-Tellera (BET). b Wartość pH roztworu wodnego h-BN-NH 2 w funkcji czasu adsorpcji CO 2 , która stopniowo maleje w wyniku wytwarzania jonów HCO 3 - . Roztwór całkowity: 100 ml wodnego roztworu nanocząstek h-BN-NH 2 o stężeniu 1 mg ml -1 . Szybkość podawania CO2 wynosi 10 ml min - 1 . c Krzywe I – V dla nanoarkuszowego roztworu wodnego h-BN-NH2 barbotowanego odpowiednio CO2 i N2 w kuwecie H. Drugą stronę zasilano wodą DI. d Model symulacyjny MD kanału agarozowego do selektywnego transportu jonów h-BN-NH 3 + i wodorowęglanowych. Rozmiar kanału ustawiono na wystarczająco szeroki, aby wyeliminować efekty rozmiaru. Względne pozycje h-BN-NH 3 + i HCO 3 - zbadano odpowiednio w t = 0 i t = 25 ns, co pokazuje, że h-BN-NH 3 + zostaje zakotwiczony, podczas gdy HCO 3 - swobodnie porusza się w obrębie i w poprzek kanał. e Energia elektrostatyczna i interakcja van der Waalsa pomiędzy agarozą i HCO 3 - w porównaniu z energiami pomiędzy agarozą i nanoarkuszem h-BN-NH 3 + . f Porównanie szybkości przenikania jonów jonów ujemnych (HCO 3 - ) i jonów dodatnich (h-BN-NH 3 + ) w gradiencie stężeń. Aby potwierdzić wyniki symulacji, zastosowano domowy zestaw dyfuzyjny z mostkiem hydrożelowym pomiędzy dwoma zbiornikami zawierającymi h-BN-NH2 i wodę DI. (dalsze szczegóły eksperymentalne podano w uwadze dodatkowej 4 ).
Aby uzyskać prąd dyfuzyjny, po uwolnieniu jonów wymagany jest selektywny kierunkowy transport jonów. Rozmiar porów matrycy hydrożelowej wynosi średnio 102 nm, czyli jest znacznie większy niż rozmiar fizyczny i promień uwodnienia (λ , ~ 4 Å ) HCO3- . Różnica wielkości znacznie zmniejsza efekty fizyczne i ładunkowe oraz obniża barierę energetyczną dla HCO 3 - ruchów w kanale jonowym. Warto zauważyć, że kanały hydrożelowe znacznie ograniczają dyfuzję jonów h-BN-NH3 + z dwóch głównych powodów. Po pierwsze, boczna wielkość nanocząstek h-BN-NH 3 + (100–300 nm) jest porównywalna z wielkością porów hydrożelu, w rezultacie nanocząstki te są fizycznie uwięzione w sieci łańcuchów hydrożelowych. Po drugie, grupy -OH w łańcuchach agarozowych mogą tworzyć silne oddziaływania z nanocząsteczkami h-BN-NH 3 + poprzez siły Van der Waalsa i oddziaływania elektrostatyczne. Obliczenia obliczeniowe wskazują, że energia interakcji łańcuchów agarozowych z nanocząstkami h-BN-NH 3 + wynosi do ~80 KJ mol -1 , podczas gdy energia interakcji jonów wodorowęglanowych osiąga wartość szczytową jedynie przy ~2,2 KJ mol -1 (rys. 3d, e , Dodatkowa ryc. 11 ). Wyniki te pokazują, że efekt wykluczenia o ograniczonym rozmiarze, w połączeniu z intensywnymi interakcjami molekularnymi połączonych trójwymiarowych wiązań wodorowych w hydrożelu, zakotwicza jony nanocząstek i poważnie ogranicza ich ruch w matrycy.
Aby uzyskać lepszy wgląd w selektywny transport jonów w hydrożelu, przeprowadzono eksperyment z dyfuzją jonów. Dwie komórki wykonanego na zamówienie urządzenia dyfuzyjnego, działające jako przedziały uwalniające/odbierające jony, zostały oddzielone mostkiem hydrożelowym służącym jako selektywny kanał jonowy. Roztwór wodny nanoarkuszów h-BN-NH2 i roztwór soli wodorowęglanu sodu, reprezentujące odpowiednio jony dodatnie i ujemne, wprowadzono oddzielnie do komory zasilającej, podczas gdy komorę odbiorczą napełniono wodą dejonizowaną (DI) (rysunek uzupełniający 12 ) . . Gradient stężeń pomiędzy dwiema komórkami spowodował, że nanocząsteczki h-BN-NH2 lub jony wodorowęglanu sodu dyfundowały z odpowiednich komórek do komórki DI-woda przez mostek hydrożelowy. Analiza ilościowa ujawniła wysoką szybkość dyfuzji jonów wodorowęglanu sodu w hydrożelu przy 0,16 mol m -2 h -1 , czyli w przybliżeniu 1,8 × 10 6 razy większą niż w przypadku nanocząstek h-BN-NH 2 w okresie testowym wynoszącym cztery dni ( D- / D + , ryc. 3f , tabela S2 i uwaga S4 ). Monitorowaliśmy także krzywe I – V roztworów wodnych h-BN-NH 2 po adsorpcji CO 2 w komórce H, z 3-krotnym gradientem stężeń oddzielonym czystym hydrożelem. Z tego wyprowadzono liczbę przeniesienia anionu (t-) bliską 1. Wynik ten dodatkowo wskazuje na prawie idealną selektywność anion/kation osiągniętą przez kanały hydrożelowe (rysunek uzupełniający 13 , uwaga 5 ). Dlatego też rozróżnialna szybkość dyfuzji jonów w sztucznych kanałach pomiędzy przeciwnie naładowanymi jonami jest podstawową zasadą 33 , 34 procesu wytwarzania energii elektrycznej indukowanego transportem jonów w naszym generatorze energii elektrycznej NAH.
Weryfikację eksperymentalną przeprowadzono również poprzez kontrolowanie długości ścieżki dyfuzji jonów, w szczególności poprzez dostosowanie szerokości czystego hydrożelu pośrodku (rysunek uzupełniający 14 ). Zmniejszenie szerokości z 3 cm do 1 cm zwiększyło pik ISC , wzrastając od 140 nA do 169,7 nA, co wskazuje na wyższy szczytowy strumień dyfuzji jonów. Co więcej, szczyt ISC osiągnął w zaledwie 11,4 min w porównaniu do 20,4 min wymaganych w prototypie 3 cm. Dodatkowo czas potrzebny do rozpadu do połowy piku I SC spadł do 24,6 min z 40,2 min. Ten przyspieszony proces ładowania i rozładowywania, osiągnięty poprzez skrócenie ścieżki dyfuzji, dobrze zgadza się z charakterystyką wytwarzania energii indukowanej dyfuzją jonów.
Praktyczna demonstracja generatora prądu NAH
Praktyczność generatora energii elektrycznej NAH została oceniona pod kątem magazynowania energii, wydajności konwersji, skalowalności, czasu reakcji i integracji modułowej. Wygenerowaną energię elektryczną można magazynować, ładując dostępny na rynku kondensator (0,5 µF) (rys. 4a ). Po podłączeniu do obwodu zewnętrznego z rezystorem 0,5 MΩ podczas cyklu adsorpcji, generator osiąga szczytową całkowitą produkcję energii wynoszącą 24 µW·h mol -1 przy gęstości objętościowej 0,0027 µW cm -3 (rys. 4b ), co odpowiada sprawność konwersji energii wynosząca około 0,6% w stosunku do całkowitej energii wejściowej ( uwagi dodatkowe 6 , 7 i rys. uzupełniająca 15 ). Chociaż sprawność konwersji energii jest zgodna z ostatnio odnotowaną wydajnością generatorów prądu wilgotnego, obecna gęstość szczytowa nie osiąga wymaganego progu 20 , 24 . Biorąc pod uwagę, że osiągnięto niemal idealną selektywność, wąskim gardłem wpływającym na obecną niską gęstość mocy wydaje się być niewystarczający strumień jonów w systemie. Dlatego też, aby poprawić gęstość mocy generatora NAH, zastosowaliśmy dwie odrębne strategie: optymalizację konfiguracji urządzenia w celu poprawy wydajności transportu jonów oraz zwiększenie zdolności adsorpcji CO2 w celu uzyskania wyższego gradientu stężeń. Te dwa podejścia pozwoliły uzyskać ogólną 10-krotną poprawę gęstości mocy. Zachęca się, aby przyszłe badania skupiały się na zwiększaniu strumienia jonów przy jednoczesnym zachowaniu wysokiej selektywności w celu dalszego zwiększenia wydajności, a tym samym utrwalenia praktycznych implikacji (rysunek uzupełniający 16 , tabela uzupełniająca 3 ).
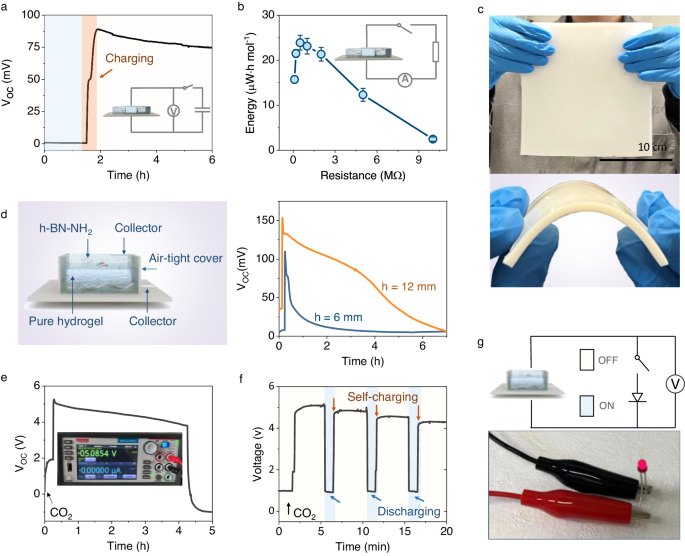
Energię elektryczną indukowaną adsorpcją CO2 magazynowano przez ładowanie dostępnego w handlu kondensatora (0,5 µF) . Niebieskie i żółte tło wskazują odpowiednio potencjał kondensatora w stanie początkowym i naładowanym. b Energia zebrana z generatora w jednym cyklu adsorpcji, gdy jest połączona z różnymi rezystorami zewnętrznymi. Całkowitą energię elektryczną obliczono zgodnie z krzywą prądu w funkcji czasu monitorowanego przez licznik źródłowy: . Słupki błędów to odchylenia standardowe z trzech testów. c Fotografie dużych rozmiarów kompozytu NAH wytworzonego metodą odlewania, przedstawiające skalowalność. d Schemat generatora ustawionego pionowo i wytwarzania energii z urządzeń o różnych grubościach (h oznacza całkowitą grubość urządzeń). Dzięki zastosowaniu generatora ustawionego pionowo, przyspieszony transport jonów prowadzi do szybkiej reakcji na CO 2 . Indukowana Voc generatorów osiągnęła swój szczyt w ciągu kilku sekund po wprowadzeniu CO2 do skrzynki testowej. Ponadto im grubszy generator, tym wyższy szczyt Voc i tym dłużej trwają sygnały elektryczne. e Wytwarzanie energii elektrycznej poprzez pięć równoległych połączeń pionowo ułożonych grup generatorów składających się z dziesięciu generatorów połączonych szeregowo (5 × 10). Wstawka przedstawia zdjęcie napięcia wyjściowego zmierzonego miernikiem źródłowym. f Do zasilania diody elektroluminescencyjnej użyto generatorów połączonych równolegle i szeregowo (5 × 10), niebieskie i czerwone tło wskazują stan przełącznika (włączony i wyłączony). Wahania rosnącej krzywej napięcia prawdopodobnie wskazują, że na prędkość ładowania wpływa charakterystyka obwodu zewnętrznego. g Zdjęcie diody emitującej (Broadcom Inc. Rozmiar żarówki: 3 mm, napięcie przewodzenia: 1,6 V, prąd przewodzenia 1 mA) zasilanej przez zintegrowane generatory CO2 .W=∫𝑅𝐼2(𝑡)𝑑(𝑡)
Aby zademonstrować skalowalność generatora energii elektrycznej NAH, wytworzono hydrożel kompozytowy NAH o wymiarach 180 mm × 180 mm × 4 mm. Następnie hydrożelową folię kompozytową pocięto na małe generatory (60 mm x 20 mm x 4 mm). Połączenie czterech z nich szeregowo lub równolegle doprowadziło do liniowego wzrostu wyjściowego V OC o około 280 mV lub ISC o około 400 nA (rys. 4c , rys. uzupełniający 17 ) . Ponieważ proces wytwarzania energii elektrycznej przez generator energii NAH jest determinowany przede wszystkim przez selektywny transport jonów w matrycy hydrożelowej NAH, prędkość wytwarzania energii elektrycznej można teoretycznie zmaksymalizować poprzez racjonalne projektowanie długości ścieżki dyfuzji jonów i efektywnego obszaru dyfuzji jonów. Aby udowodnić tę hipotezę, zaprojektowaliśmy inny typ generatora prądu NAH, w którym dwa hydrożele NAH (20 mm × 20 mm × 4 mm) umieściły czysty hydrożel o tym samym rozmiarze, ale były ułożone pionowo (ryc. 4d ). Ta konfiguracja zmniejsza długość kanału jonowego, jednocześnie zwiększając jego efektywny obszar (rysunek uzupełniający 18 ). W konfiguracji pionowej zaobserwowano raczej szybki, a nie opóźniony w czasie proces wytwarzania energii elektrycznej, skracający czas reakcji generatora energii elektrycznej NAH z minut do sekund (ryc. 4d ).
Po zintegrowaniu 50 generatorów w konfiguracji pionowej wygenerowano stabilne napięcie wyjściowe o wartości 5 V (rys. 4e ). Wygenerowana energia elektryczna wystarczyła do zasilenia diody elektroluminescencyjnej (ryc. 4g . przy napięciu roboczym 1,6 V i prądzie przewodzenia 1 mA, obejrzyj film uzupełniający 1 ). Po zapaleniu diody indukowane napięcie spadło poniżej napięcia roboczego, ale szybko powróciło do normy po odłączeniu obwodu zewnętrznego. Po czterech cyklach ładowania i rozładowania zaobserwowano jedynie niewielki spadek napięcia (rys. 4f ). To rozładowywanie i samoładowanie dodatkowo potwierdzają, że energia elektryczna wytwarzana przez urządzenie wynika z selektywnego transportu jonów. Napięcie jest budowane w wyniku przemieszczania jonów pod wpływem gradientu potencjału chemicznego. W przeciwieństwie do szybkich reakcji redoks elektrod w bateriach chemicznych, generatory energii elektrycznej indukowane transportem jonów wymagają czasu, aby przeprowadzić uwalnianie jonów i transport selektywny w celu zbudowania różnicy potencjałów.
Podsumowując, z sukcesem opracowaliśmy generatory na bazie NAH, które są w stanie wytwarzać energię elektryczną z adsorpcji CO2 . Opracowane generatory wykorzystują indukowane adsorpcją CO 2 uwalnianie jonów i separację jonów w kanałach hydrożelowych, aby ułatwić wytwarzanie energii. Nasze podejście do inżynierii jonów, obejmujące kontrolowanie ich rozmiaru fizycznego i interakcji wewnątrzcząsteczkowych, wykazuje niezwykłą skuteczność w osiąganiu ostrej separacji jonów w specjalnie zaprojektowanych kanałach. Ustalone strategie mają zastosowanie w innych różnorodnych procesach separacji jonów, obejmujących oczyszczanie, pozyskiwanie energii i odzyskiwanie zasobów. Wierzymy, że ustanowienie ram pozyskiwania energii poprzez adsorpcję CO 2 mogłoby katalizować rozwój alternatywnych rozwiązań wytwarzania energii o ujemnej emisji dwutlenku węgla, zwiększając w ten sposób zrównoważony rozwój istniejących technologii CCUS poprzez jednoczesne wychwytywanie dwutlenku węgla i konwersję energii.
Metody
Synteza nanocząstek funkcjonalizowanych PEI
Nanocząstki funkcjonalizowane PEI zsyntetyzowano przy użyciu procesu lepkiego złuszczania, jak opisano wcześniej w naszej pracy 29 . W skrócie, 0,5 g nieskazitelnych materiałów warstwowych, takich jak sześciokątny azotek boru (proszek, ~1 μm, 98%, Sigma-Aldrich), grafit (płatki, 99% węgla, Sigma-Aldrich), azotek węgla (uwaga dodatkowa 2 ) i 2 g PEI (Mn przy ~10 000 według GPC, średnia Mw przy ~25 000 według LS, Sigma-Aldrich, 408727) załadowano do 250 ml słoika do mielenia ZrO2 . Jako kule mielące wykorzystano trzy rodzaje kulek ZrO 2 o różnej masie i średnicy (100 g, d = 10 mm, 200 g, d = 5 mm i 20 g, d = 0,1 mm). Naczynie do mielenia załadowano do planetarnego młyna kulowego (ZQM-P2, Changsha Mitrcn Instrument Equipment Co., Ltd, promień obrotu: 10 cm, promień obrotu: 39 mm), a prędkość obrotową ustawiono na 250 obr/min dla obrotu i 500 obr/min dla obrotu. Po mieleniu przez ustalony czas (10 godzin, jeśli nie podano inaczej), do naczynia do mielenia dodano 100 g wody DI w celu wypłukania mieszaniny nanocząstek i PEI. Powstały roztwór wodny zawierający mieszaninę przesączono na membrany nylonowe (wielkość porów: 0,45 µm, średnica 47 mm, Sterlitech, USA) i wielokrotnie przemywano wodą, aż wartość pH wody wylotowej osiągnęła 8. Membrany nylonowe z nanocząstkami na wierzchu następnie poddano działaniu ultradźwięków przez 30 minut (Unisonics FXP12M, 40 kHz, 100 W) w celu ponownego zdyspergowania nanoarkuszy w wodzie. Na koniec dyspersję odwirowano przy RCF 236 g (Rotor 12181, Sigma 2-16 P) przez 20 minut w celu usunięcia grubych płatków. Supernatant zdekantowano jako końcowy produkt dyspersji wodnej nanocząstek funkcjonalizowanych PEI.
Produkcja generatorów
Proszek agarozowy (Sigma-Aldrich, BioReagent, temperatura żelowania 36°C ± 1,5°C) rozpuszczono w wodzie o temperaturze 80°C w celu otrzymania roztworów prekursora hydrożelu o stężeniach receptywności 2% wag. i 4% wag. i przechowywano w temperaturze Piec o temperaturze 70°C do produkcji generatorów. Wycięto ogniwo gumowe PDMS (Sylgard 184, Dow Corning) o wymiarach 6 mm x 2 mm x 0,4 mm i zastosowano je jako formę generatora. Odbieraki prądu utworzono poprzez pokrycie srebrną farbą dolnej części dwóch końców ogniwa PDMS. Jako odbieraki prądu zastosowano również taśmę węglową i platynowaną siatkę tytanową (Sklep z ogniwami paliwowymi, 592770). Po osadzeniu kolektorów elektrycznych, czysty roztwór agarozy (2% wag.) w temperaturze 70 ° C najpierw wlano kroplowo do formy PDMS i pozostawiono w atmosferze na 30 minut, aby przejść przejście zol-żel w celu utworzenia folii hydrożelowej. Następnie wygrawerowano dwa końce czystej folii hydrożelowej (2 mm x 2 mm x 0,4 mm), pozostawiając w formie tylko środkową część. Po drugie, roztwór nanocząstek o stężeniu 2 mg ml -1 (o ile nie podano inaczej) ogrzano do 70°C i zmieszano z równą objętością roztworu prekursora agarozy o stężeniu 4% wag. Otrzymany roztwór mieszanki wlano kroplowo na dwa końce formy PDMS i pozostawiono na kolejne 30 minut, aby ostatecznie otrzymać 3-modułowy generator NAH. W przypadku całego generatora NAH roztwór mieszaniny agarozy i nanoarkuszów wlano bezpośrednio do odpowiedniej formy bez procedury odlewania czystego roztworu agarozy. Urządzenie następnie podłączono do obwodu zewnętrznego wyposażonego w miernik źródłowy (Keithley 2450) w celu monitorowania sygnałów elektrycznych generatora podczas testów.
Pomiary elektryczne
Napięcie obwodu otwartego i prąd zwarciowy generatora kompozytowego NAH mierzono za pomocą miernika źródłowego (Keithley 2450) w warunkach otoczenia. Test wyjścia prądowego ustawiono na 0 nA, a napięcie na 0 V odpowiednio dla pomiarów obwodu otwartego i zwarcia. Generator umieszczono w skrzyni testowej (50 cm na 25 cm) z wlotem CO 2 na dole i wylotem na górze, a dwa kolektory po lewej/prawej stronie połączono poprzez obwód zewnętrzny w celu rozładowania urządzenia dopóki ISC nie spadnie poniżej 5 nA. Ten proces wstępnego rozładowania pomógł zredukować wpływ niewielkich różnic potencjałów chemicznych w kompozycie hydrożelowym, spowodowanych sztucznie wprowadzoną asymetryczną strukturą. Następnie do skrzynki wprowadzono CO2 przy natężeniu przepływu 2,5 l / min -1 przez 3 minuty, po czym urządzenie przykryto w celu dalszych testów. Aby ocenić gęstość mocy, generator połączono z zewnętrznymi rezystorami o różnej rezystancji i monitorowano prąd zewnętrzny w celu obliczenia gęstości. Krzywe IV roztworu wodnego nanoarkusza uzyskano przy użyciu pary elektrod Ag/AgCl przy przyłożonych napięciach w zakresie od -0,2 V do 0,2 V.
Regeneracja generatora
Zbadano regenerację generatora, wybierając strategię zmiany pH, aby zbadać jego potencjał wielokrotnego wykorzystania 25 . Po 5 cyklach wytwarzania energii elektrycznej generator wyjęto i zanurzono w roztworze wodorotlenku wapnia (Ca(OH) 2, > 95%, Sigma-Aldrich) o wartości pH 10 na 1 godzinę. Następnie 3-krotnie przemyto generator nadmiarem wody DI. Następnie generator umieszczono z powrotem w komorze testowej i poddano tym samym procedurom testowym.
Charakterystyka materiałów
Strukturę sieciową hydrożelu agarozowego i generatora kompozytu analizowano różnymi metodami. Strukturę sieciową hydrożelu agarozowego i generatora kompozytu badano za pomocą skaningowego mikroskopu elektronowego (SEM) (Nova NanoSEM 450, FEI, USA) pracującego przy napięciu 3 kV i odległości roboczej 5 mm. W celu przygotowania próbek hydrożel zanurzano najpierw w ciekłym azocie w celu szybkiego zamrożenia struktury, a następnie poddano liofilizacji (FreeZone 2,5 litra, Labconco Corporation, USA). Otrzymane próbki pokryto irydem (o grubości 1,5 do 2 nm) przed charakteryzacją SEM. Zawartość pierwiastków (C, N i H) w próbkach oznaczono za pomocą analizatora pierwiastkowego (FlashSmart, Thermo Scientific) przy użyciu próbek proszku (liofilizowanych z wodnego roztworu nanoarkusza). Rentgenowską spektroskopię fotoelektronów (XPS) przeprowadzono przy użyciu próbek proszku h-BN w systemie analizy powierzchni Thermo Scientific Nexsa wyposażonym w analizator półkulisty. Analizę dyfrakcji rentgenowskiej (XRD) przeprowadzono w temperaturze od 5 do 100°C za pomocą dyfraktometru wyposażonego w promieniowanie Cu Kα (dyfraktometr rentgenowski Miniflex 600, Rigaku, Japonia; dyfraktometr proszkowy D2 PHASER, Bruker, Niemcy) przy użyciu proszku h- Próbka nanoarkusza BN i h-BN. TGA przeprowadzono w zakresie od 50 do 900°C z szybkością wzrostu temperatury 10°C min -1 w ciągłym przepływie azotu (PerkinElmer TGA 8000).
Badanie symulacyjne dynamiki molekularnej (MD).
Do porównania zachowania transportowego jonów HCO 3 - i h-BN-NH 3 + przez kanał agarozowy o średnicy kanału 8 nm zastosowano symulację MD. Układy napełniono wodą w procesie solwatacji. Cząsteczki wody opisano modelem SPC/E 35 . Uniwersalne pole siłowe UFF Forcefield 36 z ładunkiem QEq jest przypisane do h-BN-NH 3 + 37 i innych cząsteczek poprzez kody Open Babel 38 i OBGMX 39 . Arkusz BN został zamrożony w symulacjach podczas procesu symulacji. Systemy poddano wieloetapowej minimalizacji energii przy najbardziej stromym zniżaniu, a następnie minimalizacji energii CG. Następnie przeprowadzono symulacje równowagi 100 ps NVT i symulacje równowagi 100 ps NPT. Krok czasowy wynosi 2,0 fs, a wiązania z atomami wodoru utrzymywano za pomocą algorytmu LINCS 40 . Termostat V-rescale utrzymywał stałą temperaturę symulacyjną 298,15 K, a połączenie ciśnieniowe osiągnięto poprzez Parrinello-Rahmana 41 . Rcoulomb i rvdw ustalono na 10 Å. Do oceny oddziaływań elektrostatycznych wykorzystano algorytm siatki cząstek Ewalda. Następnie przeprowadzono symulację produkcji trwającą 50 ns. Wszystkie symulacje MD w tej pracy przeprowadzono przy użyciu GROMACS 2019.6 42 . Wyniki symulacji zostały przeanalizowane i wygenerowane przy użyciu oprogramowania VMD (VMD dla WIN64, wersja 1.9.3, 6 września 2020) 43 .
Dostępność danych
Wszystkie dane zawarte w tym badaniu znajdują się w tym artykule i jego pliku informacji uzupełniających. Surowe dane można uzyskać od autora na życzenie. Do artykułu załączono dane źródłowe .
Bibliografia
-
IPCC, „ Zmiany klimatyczne 2014: łagodzenie zmian klimatycznych ” 41–47 https://www.ipcc.ch/site/assets/uploads/2018/02/ipcc_wg3_ar5_full.pdf (Cambridge University Press, 2014).
-
Międzynarodowa Agencja Energetyczna, „ CO 2 emisji z paliw spalania podkreśla ” 9–21 https://emis.vito.be/sites/emis.vito.be/files/articles/3331/2016/CO2EmissionsfromFuelCombustion_Highlights_2016.pdf (Międzynarodowa Agencja Energetyczna, 2016).
-
Rhodes, CJ Konferencja klimatyczna w Paryżu w 2015 r.: COP21. Nauka. Wałówka. 99 , 97–104 (2016).
-
Cohen, R., Eames, PC, Hammond, GP, Newborough, M. i Norton, B. Pakt klimatyczny z Glasgow z 2021 r. – kroki na ścieżce przejścia w kierunku świata niskoemisyjnego. Proc. Inst. cywil. Inż.: Energia 3 , 97–102 (2022).
-
Bui, M. i in. Wychwytywanie i składowanie dwutlenku węgla (CCS): przyszłość. Środowisko Energetyczne. Nauka. 11 , 1062–1176 (2018).
-
Wei, Y.-M. i in. Proponowany globalny układ wychwytywania i składowania dwutlenku węgla zgodny z celem klimatycznym wynoszącym 2°C. Nat. Klim. Zmień 11 , 112–118 (2021).
-
Wilberforce, T., Olabi, A., Sayed, ET, Elsaid, K. i Abdelkareem, MA Postęp w technologiach wychwytywania dwutlenku węgla. Nauka. Całkowite środowisko. 761 , 143203 (2021).
-
Kim, EJ i in. Spółdzielcze wychwytywanie węgla i regeneracja pary za pomocą struktur metaloorganicznych z dodatkiem tetraaminy. Nauka 369 , 392–396 (2020).
-
Hanssen, S. i in. Potencjał bioenergii w zakresie łagodzenia zmiany klimatu poprzez wychwytywanie i składowanie dwutlenku węgla. Nat. Klim. Zmień 10 , 1023–1029 (2020).
-
Goeppert, A. i in. Wychwytywanie dwutlenku węgla z powietrza za pomocą regenerowalnego stałego adsorbentu na bazie poliaminy. J. Am. Chem. Towarzystwo 133 , 20164–20167 (2011).
-
Doyle, DA i in. Struktura kanału potasowego: molekularne podstawy przewodnictwa i selektywności K+. nauka 280 , 69–77 (1998).
-
Xiao, K., Jiang, L. i Antonietti, M. Transport jonów w urządzeniach nanofluidycznych do pozyskiwania energii. Dżul 3 , 2364–2380 (2019).
-
Gouaux, E. i MacKinnon, R. Zasady selektywnego transportu jonów w kanałach i pompach. nauka 310 , 1461–1465 (2005).
-
Shen, J., Liu, G., Han, Y. i Jin, W. Sztuczne kanały do zamkniętego transportu mas w skali poniżej nanometra. Nat. Ks. Mater. 6 , 294–312 (2021).
-
Zhang, P. i in. Kowalencyjna membrana nanofluidyczna o strukturze organicznej jako platforma dla bardzo czułej termosensacji bionicznej. Nat. komuna. 12 , 1844 (2021).
-
Yang, G. i in. Ultracienka membrana Ti3C2Tx (MXene) do wytwarzania energii elektrokinetycznej pod ciśnieniem. Nano Energy 75 , 104954 (2020).
-
Qin, S. i in. Nanofluidyczne generatory elektryczne zbudowane z membran nanocząstek azotku boru. Nano Energy 47 , 368–373 (2018).
-
Yang, J. i in. Postęp w wytwarzaniu energii osmotycznej przez monowarstwę kowalencyjnej struktury organicznej. Nat. Nanotechnologia. 17 , 622–628 (2022).
-
Kim, S. i in. Neuromorficzne kryształy van der Waalsa do wytwarzania znacznej energii. Nat. komuna. 12 , 1–10 (2021).
-
Liu, X. i in. Wytwarzanie energii z wilgoci otoczenia za pomocą nanodrutów białkowych. Natura 578 , 550–554 (2020).
-
Zhao, F., Cheng, H., Zhang, Z., Jiang, L. i Qu, L. Bezpośrednie wytwarzanie energii z warstwy tlenku grafenu pod wpływem wilgoci. Adw. Matko. 27 , 4351–4357 (2015).
-
Zhu, R. i in. Zwiększanie wytwarzania energii elektrycznej z tlenku grafenu wywołanego wilgocią poprzez inżynierię grup funkcyjnych na bazie tlenu. Nano Energy 94 , 106942 (2022).
-
Wang, L. i in. Aktywny transport protonów napędzany światłem przez membrany tlenku grafenu janusowego domieszkowane fotokwasem i fotozasadą. Adw. Matko. 31 , 1903029 (2019).
-
Wang, H. i in. Dwuwarstwowa folia polielektrolitowa do spontanicznego wytwarzania energii w powietrzu do zintegrowanego napięcia wyjściowego 1000 V. Nat. Nanotechnologia. 16 , 811–819 (2021).
-
Kang, JM i in. Energooszczędna regeneracja chemiczna AMP z wykorzystaniem wodorotlenku wapnia do obsługi procesu wychwytywania dwutlenku węgla. Chem. inż. J. 335 , 338–344 (2018).
-
Chen, C. i in. Nanofluidyczne wytwarzanie energii osmotycznej z CO2 za pomocą membran celulozowych. Zielony. Węgiel 1 , 58–64 (2023).
-
Prajapati, A. i in. Wspomagany migracją proces gradientu wilgoci umożliwiający ultraszybkie, ciągłe wychwytywanie CO 2 z rozcieńczonych źródeł w warunkach otoczenia. Środowisko Energetyczne. Nauka. 15 , 680–692 (2022).
-
Lv, B., Guo, B., Zhou, Z. i Jing, G. Mechanizmy wychwytu CO2 do roztworu monoetanoloaminy przy różnym obciążeniu CO2 podczas procesów absorpcji/desorpcji. Otaczać. Nauka. Techn. 49 , 10728–10735 (2015).
-
Wang, Z. i in. Skalowalna, wysokowydajna eksfoliacja dla jednowarstwowych nanoarkuszów. Nat. komuna. 14 , 236 (2023).
-
Lei, W. i in. Roztwory koloidalne azotku boru, ultralekkie aerożele i wolnostojące membrany poprzez jednoetapową eksfoliację i funkcjonalizację. Nat. komuna. 6 , 8849 (2015).
-
Roberts, JJ, Earnshaw, A., Ferguson, VL i Bryant, SJ Badanie porównawcze lepkosprężystego zachowania mechanicznego hydrożeli agarozowych i poli(glikolu etylenowego). J. Biomed. Matko. Rozdzielczość Część B 99 , 158–169 (2011).
-
Jin, S., Wu, M., Gordon, RG, Aziz, MJ i Kwabi, DG Cykl zmiany pH do wychwytywania CO2 napędzany elektrochemicznie poprzez transfer elektronów sprzężony z protonami. Środowisko Energetyczne. Nauka. 13 , 3706–3722 (2020).
-
Cao, L. i in. Olbrzymia konwersja energii osmotycznej poprzez ustawione pionowo, selektywnie przepuszczające jony nanokanały w kowalencyjnych membranach organicznych. J. Am. Chem. Towarzystwo 27 , 12400–12409 (2022).
-
Tunuguntla, RH i in. Zwiększona przepuszczalność wody i regulowana selektywność jonowa w porinach nanorurek węglowych o wielkości poniżej nanometra. Nauka 357 , 792–796 (2017).
-
Berendsen, H., Grigera, J. i Straatsma, T. Brakujący termin w efektywnych potencjałach par. J.Fiz. Chem. 91 , 6269–6271 (1987).
-
Rappe, AK i in. UFF, pełne pole sił układu okresowego do symulacji mechaniki molekularnej i dynamiki molekularnej. J. Am. Chem. Towarzystwo 114 , 10024–10035 (1992).
-
Warner, JH i in. Dynamika paramagnetycznych metalofullerenów w grochach nanorurek węglowych. Nano Lett. 8 , 1005–1010 (2008).
-
O'Boyle, NM i in. Otwórz Babel: Otwarty zestaw narzędzi chemicznych. J.Cheminform. 3 , 1–14 (2011).
-
Garberoglio, G. OBGMX: Internetowy generator topologii GROMACS dla układów molekularnych i okresowych wykorzystujących uniwersalne pole siłowe. J. Oblicz. Chem. 33 , 2204–2208 (2012).
-
Hess, B., Bekker, H., Berendsen, HJC i Fraaije, JGEM LINCS: Narzędzie do rozwiązywania ograniczeń liniowych do symulacji molekularnych. J. Oblicz. Chem. 18 , 1463–1472 (1997).
-
Feller, SE, Zhang, Y., Pastor, RW i Brooks, BR Symulacja dynamiki molekularnej przy stałym ciśnieniu: Metoda tłokowa Langevina. J.Chem. Fiz. 103 , 4613–4621 (1995).
-
Abraham, G. Wysokowydajne symulacje molekularne poprzez wielopoziomową równoległość od laptopów po superkomputery. Oprogramowanie X 1 , 19–25 (2015).
-
Humphrey, W., Dalke, A. i Schulten, K. VMD: wizualna dynamika molekularna. J. Mol. Wykres. 14 , 33–38 (1996).
Podziękowanie
Dziękujemy Yun Xia, Zhonghao Xu i Xin Zeng za projektowanie i rysowanie grafik. Dziękujemy za wsparcie finansowe ze strony Centrum Doskonałości ARC ds. Zielonej Elektrochemicznej Transformacji Dwutlenku Węgla (CE230100017) oraz Centrum Badań nad Transformacją Przemysłu ARC w zakresie energooszczędnej separacji (IH170100009). XWZ dziękuje Australijskiej Radzie ds. Badań Naukowych za stypendium ARC Future Fellowship (FT210100593). W pracy tej wykorzystano obiekty Monash Center for Electron Microscopy (MCEM) i Melbourne Center for Nanofabrication (MCN).






