Już dawno pisaliśmy o tym, narkolepsja została wywołana takim precyzyjnie wybiórczym czy losowym podrzuceniem trucizn do szczepionki p. świńskiej grypie wywołującej to potworne schorzenie.
Jesteśmy mordowani.
Red. Gazeta Warszawska
+
Badanie przeprowadzone w Danii pokazuje: Poszczególne partie tak zwanej „szczepionki Covid-19” firmy Pfizer Comirnaty (BNT162b2) mają szczególnie problematyczny profil bezpieczeństwa. Wynika to z kumulacji ciężkich działań niepożądanych. Różnice w stosunku do mniej problematycznych partii są statystycznie niezwykle istotne. W normalnych okolicznościach sam fakt istnienia tych różnic byłby znakiem ostrzegawczym i powodem do wycofania produktu. Ale co gorsza: wydaje się, że są wspólnicy.
Badanie, które ma potencjał kryminalistyczny, można znaleźć pod nazwą Batch-dependent safety of the BNT162b2 mRNA COVID-19 szczepionka . Zaangażowani naukowcy to Duńczycy Max Schmeling, Vibeke Manniche i Peter Riis Hansen.
Przede wszystkim należy zauważyć, że w samej Europie na dzień 11 listopada 2022 r. zgłoszono 971 021 poważnych zdarzeń niepożądanych. Podejście dochodzenia krótko wyjaśnił:
Jednak nie tylko w odniesieniu do awaryjnego zatwierdzania rynku i szybkiego wdrażania programów szczepień na dużą skalę, możliwość zmiany zależnej od partii wydaje się warta zbadania.
Badanie „Zależne od partii bezpieczeństwo szczepionki BNT162b2 mRNA COVID-19”
Dochodzenie dotyczy zgłoszeń skutków ubocznych w Danii od 27 grudnia 2020 r. do 11 stycznia 2022 r. Są one rejestrowane w państwowej bazie danych bezpieczeństwa DKMA i klasyfikowane według ciężkości. Numer partii jest tam również zapisywany wraz z raportami o podejrzanej aktywności. Klasyfikacja obejmuje: nieciężkie, ciężkie (z hospitalizacją, chorobą zagrażającą życiu, trwałym kalectwem lub wrodzonymi wadami rozwojowymi) i zgon.
Łącznie podano 7 835 280 dawek 3 748 215 osobom stosującym 52 różne partie szczepionki BNT162b2 (2 340-814 320 dawek na partię), a u 13 635 osób zarejestrowano 43 496 poważnych działań niepożądanych.
W sumie 66 587 skutków ubocznych zostało rozłożonych na 52 partie, co oznacza, że po podaniu wielu dawek osoby cierpiały i za każdym razem rejestrowano poważne skutki uboczne.
Ocena tych danych umożliwiła, po wykluczeniu wszystkich zgłoszeń bez numerów serii, przypisanie 61 847 zgłoszonych poważnych działań niepożądanych do odpowiednich serii. Spośród poważnych skutków ubocznych 14 509 (23,5 procent) zostało sklasyfikowanych jako poważne, a 579 (0,9 procent) jako śmiertelne.
Świńska grypa, Pandemrix i narkolepsja
- Opublikowano: 20 listopada 2020 r
- Ostatnia aktualizacja: 20 listopada 2020 r
Szczepienie szczepionką Pandemrix przeciwko świńskiej grypie w latach 2009–2010 przyczyniło się do zwiększonego ryzyka wystąpienia narkolepsji u dzieci i młodych dorosłych. Narkolepsja jest chorobą autoimmunologiczną, na którą narażone są osoby z pewnymi predyspozycjami genetycznymi. Nadal nie jest jasne, co w szczepionce spowodowało zwiększone ryzyko narkolepsji.
Pandemia oznacza, że zaraźliwa, poważna choroba szybko rozprzestrzenia się między kilkoma częściami świata. W kwietniu 2009 r. w Meksyku i Stanach Zjednoczonych odnotowano ognisko grypy A/H1N1 (zwanej także świńską grypą ). Choroba szybko się rozprzestrzeniała i uznano, że może powodować poważne choroby w niektórych grupach, zwłaszcza u młodszych osób. W czerwcu 2009 roku Światowa Organizacja Zdrowia (WHO) uznała wybuch za pandemię. 1
Zatwierdzenie szczepionki pandemicznej
W Szwecji władze i służba zdrowia współpracują ze sobą, aby móc szybko podjąć środki zapobiegawcze w przypadku wybuchu epidemii chorób zakaźnych, gdzie jednym z takich środków są szczepienia.
Pandemrix został zatwierdzony w 2008 roku jako szczepionka pandemiczna w UE zgodnie z aktualnymi wymogami dotyczącymi skuteczności i bezpieczeństwa. Zatwierdzenie opierało się między innymi na testach na około 5000 ochotników. 2
Pandemrix był tak zwaną szczepionką prototypową , zaprojektowaną zgodnie z tą samą zasadą, co zwykłe szczepionki przeciw grypie. Przed każdym sezonem grypowym inaktywowana substancja zakaźna, zwana antygenem, jest zastępowana w szczepionce, aby odpowiadała obecnym typom wirusów grypy sezonowej. Szczepionki przeciw grypie zwykle zawierają 3–4 szczepów wirusa, podczas gdy Pandemrix zawierał tylko antygen z jednego szczepu wirusa. W przeciwieństwie do szczepionek przeciwko zwykłej grypie sezonowej szczepionka Pandemrix zawierała również substancję (adiuwant) zapewniającą zwiększoną ochronę.
Pandemrix przeciwko grypie A/H1N1 został zatwierdzony przez Komisję UE- 29 września 2009 r., aw październiku pierwsi mieszkańcy Szwecji mogli otrzymać szczepionkę. 4 Dalsze badania dotyczące różnych grup ryzyka i dzieci zostały przeprowadzone i ocenione jesienią 2009 roku.
Realizacja szczepienia
W okresie od października 2009 r. do kwietnia 2010 r. szczepionką Pandemrix w Szwecji zaszczepiono około 5,3 miliona osób, co stanowi około 60% populacji. W UE zaszczepiono łącznie 30,8 miliona osób w 19 krajach UE/EOG.
W ocenie przeprowadzonej w 2013 r. Instytut Kontroli Chorób Zakaźnych ocenił, że szczepienie zaowocowało w całym kraju uniknięciem około 100 zgonów i nieco ponad 200 przypadków intensywnej terapii, a także około 1750 pacjentów hospitalizowanych. 6
Zgłaszanie podejrzewanych działań niepożądanych
Od czasu rozpoczęcia szczepień w Szwecji w październiku 2009 r. do ich zakończenia wiosną 2010 r. zachęcano zarówno służbę zdrowia, jak i społeczeństwo do zgłaszania podejrzewanych skutków ubocznych. Kompilacje otrzymanych zgłoszeń były na bieżąco publikowane na stronie internetowej Szwedzkiej Agencji Leków.
W maju 2010 r. Szwedzka Agencja Leków opublikowała zestawienie wszystkich zgłoszonych podejrzewanych działań niepożądanych w Szwecji w okresie od października 2009 r. ponad 2000 od pacjentów/ogółu społeczeństwa. 3
Zgłoszenia były zgodne z tym, co wykazały badania kliniczne i czego zwykle oczekuje się po szczepieniu, np. reakcje w miejscu wstrzyknięcia (tkliwość, obrzęk, zaczerwienienie) lub objawy ogólnoustrojowe, takie jak stan zapalny, gorączka i ból głowy. Są to spodziewane reakcje układu odpornościowego organizmu podczas szczepienia. W momencie kompilacji nie zgłoszono żadnego przypadku narkolepsji jako podejrzewanego działania niepożądanego.
Zgłoszone przypadki narkolepsji
Latem 2010 roku otrzymano kilka zgłoszeń o podejrzeniu przypadków narkolepsji u dzieci i młodzieży w Szwecji po szczepieniu. Liczba zgłoszonych podejrzeń zachorowań w wieku do 19 lat przekroczyła oczekiwaną częstość występowania narkolepsji w tej grupie wiekowej. W tym samym czasie podobny sygnał dotyczący skutków ubocznych otrzymano z Finlandii.
W sierpniu 2010 r. Europejska Agencja Leków EMA na wniosek Komisji UE- rozpoczęła dochodzenie w sprawie możliwego związku przyczynowego między Pandemrixem a narkolepsją. EMA oceniła, że nie można nawiązać połączenia, ale konieczne są dalsze badania. 13
Zarówno Szwecja, jak i Finlandia przeprowadziły badania rejestrowe w 2010 i 2011 r., które potwierdziły możliwy związek między szczepieniem szczepionką Pandemrix a wystąpieniem narkolepsji. 7,9 Wyniki tych badań przyczyniły się do zmiany przez EMA zaleceń dotyczących stosowania szczepionki Pandemrix w lipcu 2011 roku. 12 Szczepionka została wyrejestrowana w sierpniu 2015 r.
Duże badanie wykazało zwiększone ryzyko
Szwedzka Agencja Leków podjęła również inicjatywę przeprowadzenia innych badań w celu bardziej szczegółowej oceny wzrostu ryzyka, rzucenia światła na możliwe mechanizmy działania i zbadania czasu między szczepieniem a chorobą.
W marcu 2013 r. zaprezentowano kompleksowe badanie przeprowadzone przez Szwedzką Agencję Leków, Karolinska Institutet oraz siedem rad powiatów i regionów, w którym porównano dane rejestrowe dotyczące 3,3 mln osób zaszczepionych i 2,5 mln osób nieszczepionych w okresie od października 2009 r. do grudnia 2011 r. Celem było w celu oceny ryzyka wystąpienia chorób neurologicznych lub o podłożu immunologicznym i autoimmunologicznym po szczepieniu szczepionką Pandemrix.
W badaniu odnotowano około trzykrotny wzrost ryzyka zachorowania na narkolepsję po zastosowaniu szczepionki Pandemrix w grupie wiekowej 0–19 lat. W grupie wiekowej 20–29 lat zaobserwowano podwojenie ryzyka, aw starszych grupach wiekowych brak gwarancji wzrostu ryzyka. W badaniu nie wykazano wzrostu ryzyka innych chorób neurologicznych lub autoimmunologicznych. 11
Liczbę ofiar trudno oszacować
Do 2020 r. do Szwedzkiej Agencji Leków zgłoszono łącznie 394 przypadki narkolepsji jako podejrzewanego działania niepożądanego po szczepieniu szczepionką Pandemrix. Ponieważ osoby mogą cierpieć na narkolepsję niezależnie od tego, czy były szczepione szczepionką Pandemrix, czy nie, nie jest możliwe ustalenie indywidualnych powiązań ze szczepieniem.
Liczba zgłoszonych podejrzewanych działań niepożądanych, liczba pacjentów złapanych poprzez rejestrację w systemie dokumentacji medycznej oraz liczba pacjentów, którzy otrzymali odszkodowanie z Läkemedelsförsäkringen, jest różna. Fakt, że informacje z różnych źródeł są podawane jako miara liczby zachorowań, oznacza, że liczby mogą się różnić i prowadzić do nieporozumień. Ponieważ ryzyko zachorowania zmniejsza się z czasem po szczepieniu, wybór okresu ma również znaczenie dla sposobu obliczania ryzyka i liczby przypadków.
Po uwzględnieniu normalnego występowania narkolepsji Szwedzka Agencja Leków szacuje, że około 150–200 osób cierpiało na narkolepsję w wyniku szczepienia szczepionką Pandemrix.
Co to jest narkolepsja?
Narkolepsja jest zaburzeniem neurologicznym, w którym mózg nie może kontrolować czuwania i snu. Oznacza to, że osoby z tą chorobą stają się bardzo zmęczone w ciągu dnia i mają napady snu, którym nie można zapobiec. Do objawów należy również katapleksja, czyli nagła bezsilność i uczucie paraliżu w połączeniu z emocjami takimi jak radość i złość.
Choroba znana jest od końca XIX wieku. Dokładna częstość występowania obecnie nie jest jasna, ale oczekuje się jednego nowego przypadku na 100 000 osób rocznie. Szacuje się, że w Szwecji żyje 4500 osób z narkolepsją. 5
Długi czas między objawami a diagnozą
Objawy zmęczenia związane z narkolepsją często pojawiają się przez długi czas. Utrudnia to ocenę systemu opieki zdrowotnej i może prowadzić do opóźnionej diagnozy.
W badaniu, które Szwedzka Agencja Leków opublikowała w czerwcu 2016 r., zbadano dane rejestrowe od około 200 osób, które zostały zaszczepione szczepionką Pandemrix i później rozwinęła się narkolepsja. Średni czas od pierwszego zgłoszenia przez pacjenta objawów do późniejszego rozpoznania narkolepsji wynosił średnio 67 tygodni, w niektórych przypadkach ponad dwa lata. 8
Co powoduje narkolepsję?
Od 2010 roku Szwedzka Agencja Leków koordynowała szereg badań, aby rzucić światło na możliwe mechanizmy odpowiedzialne za wystąpienie narkolepsji. Przeprowadzone badania nie były w stanie wykazać żadnego pojedynczego czynnika w szczepionce, który mógłby wyjaśnić początek narkolepsji. Czynniki dziedziczne istotne dla układu odpornościowego, jak również narażenie na sam wirus grypy, zostały wskazane jako możliwe czynniki leżące u podstaw. Jednym z takich czynników dziedzicznych jest tkanka HLA typu DQB1 0602, którą posiadają wszyscy chorzy na cięższą postać narkolepsji.
Niedawne badania nad przyczynami narkolepsji wykazały, że istnieją podobieństwa między strukturami wirusa grypy A/H1N1 i komórek w mózgu, które wytwarzają substancję hipokretynę (oreksynę), która jest niezbędna do regulacji snu organizmu. Prowadzi to do tego, że własny układ odpornościowy jest w stanie zaatakować te komórki i zablokować produkcję hipokretyny, czego konsekwencją jest narkolepsja. 14
Krótko o Pandemrixie i narkolepsji
- Narkolepsja to niezwykła choroba, której zdiagnozowanie może zająć dużo czasu, ponieważ objawy mogą się różnić u poszczególnych osób i początkowo mogą być łagodne.
- Testy i badania, które poprzedziły zatwierdzenie szczepionki Pandemrix w UE, spełniły wszystkie wymagania dotyczące skuteczności i bezpieczeństwa szczepionek pandemicznych.
- W badaniach klinicznych, które należy przeprowadzić, zanim lek zostanie dopuszczony do obrotu, odkrywa się zarówno powszechne, jak i mniej powszechne działania niepożądane. Narkolepsja po szczepieniu szczepionką Pandemrix jest bardzo rzadkim działaniem niepożądanym (odpowiednik <1 przypadku na 10 000 zaszczepionych) i nawet dzisiaj bardzo trudno byłoby ją wykryć w badaniach klinicznych przeprowadzanych przed zatwierdzeniem szczepionki.
- Wciąż niepełna jest wiedza na temat przyczyn zachorowania na narkolepsję, a także tego, co w szczepieniu, szczepionce i reakcjach poszczególnych osób miało wpływ na zwiększone ryzyko zachorowania.
- Zgłaszanie podejrzewanych działań niepożądanych jest ważne dla identyfikacji sygnałów dotyczących bezpieczeństwa. Jednak aby móc określić przyczynowość i wielkość ryzyka rzadkich działań niepożądanych, potrzebne są dogłębne badania ze szczegółowymi informacjami zarówno na temat szczepienia, jak i stanu chorobowego.
Wynik wskazuje na współudział
Naukowcy oczekiwaliby, że „jakość” szczepionki będzie w dużej mierze identyczna we wszystkich partiach, a zatem występowanie skutków ubocznych będzie równomiernie rozłożone. Tego można by się również spodziewać po odpowiednio zatwierdzonej i przetestowanej substancji czynnej. Wynik był tym bardziej zaskakujący.
Jednak liczba zgłoszonych poważnych działań niepożądanych różniła się znacznie w zależności od serii szczepionki i wahała się od 0,09 do 3,59 na 1000 podanych dawek. Ta różnica jest dramatyczna i można ją wytłumaczyć jedynie skrajnie różną jakością szczepionek.
Problem, który wskazuje na dalszą działalność przestępczą, polega na tym, że partie, w których wystąpiła szczególnie duża liczba poważnych skutków ubocznych, były rzadziej opryskiwane. Jest to właściwie możliwe tylko wtedy, gdy ktoś przerwał szczepienie lub rzadziej rozdawał te partie. Kto był świadomy zagrożeń i kto zainicjował te działania? Czy to było państwo? Czy to był producent?
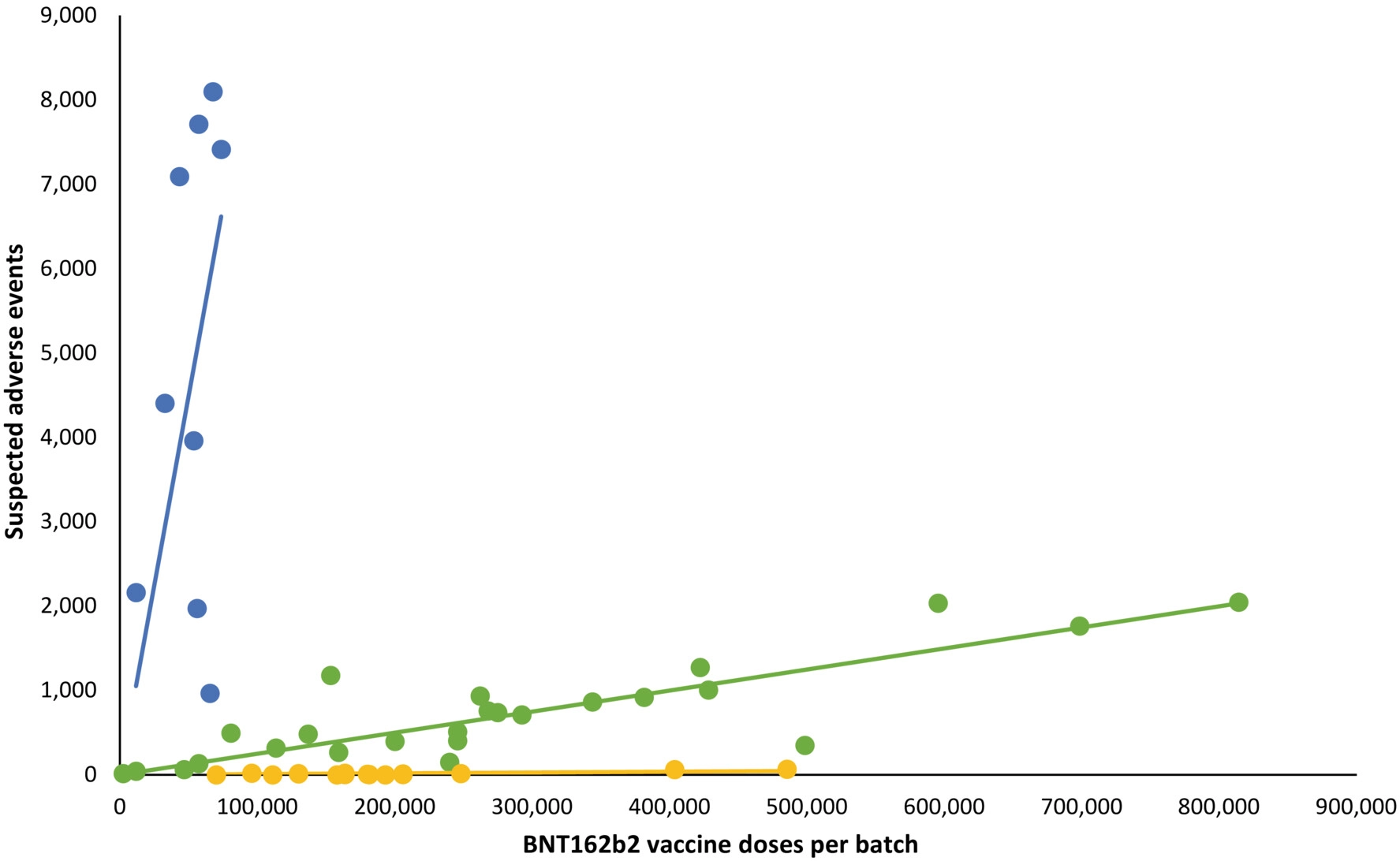
Problem – jak ze wszystkim, co pochodzi z danych z baz danych skutków ubocznych – polega na tym, że jest to tylko zbiór dobrowolnych wpisów. Wiemy o niedoszacowaniu w zakresie od 99 do 90 procent wszystkich skutków ubocznych na całym świecie. Tych z różnych powodów nigdy nie złożono, między innymi dlatego, że nie ma takiego obowiązku, ale także dlatego, że lekarze nie otrzymują wynagrodzenia za tę żmudną pracę. Dlatego można założyć pewną „stronniczość raportu”.
Zespół naukowy zwraca również uwagę, że według jego wiedzy w Danii nie wycofano ani jednej partii szczepionki Comirnaty.
Podsumowując, wyniki sugerują istnienie zależnego od serii sygnału bezpieczeństwa dla szczepionki BNT162b2 i uzasadnione są dalsze badania w celu zbadania tej wstępnej obserwacji i jej implikacji.
Wnioski z badania „Zależne od partii bezpieczeństwo szczepionki BNT162b2 mRNA COVID-19”
kkkkkkkkkkkkkkkkkkkkkkkkkkkkkkkkkkkkkkk
https://report24.news/besonders-toedliche-impfchargen-wurden-seltener-verspritzt-wer-wusste-bescheid/#:~:text=Badanie%20przeprowadzone%20w,UBOCZNE%20%2C%20PFIZER







